Давайте представим себе лабораторию будущего, где вместо рядов пробирок и чашек Петри буду пластиковые картриджи размером с флешку, внутри которых пульсируют миниатюрные версии человеческих органов. Вот так выглядит технология «орган-на-чипе» (organ-on-a-chip, OOAC), которую сейчас активно развивают.

Почему переходят к технологии «орган-на-чипе»?
На протяжении десятилетий ученые полагались на два основных метода: выращивание клеток в 2D-культурах и эксперименты на животных. Оба подхода имеют ограничения.
2D-культуры, хотя просты и дешевы, не способны воспроизвести сложную трехмерную архитектуру тканей, межклеточные взаимодействия и механические силы, существующие в живом организме. Клетки в них неестественно уплощаются, теряют свою специфическую форму и по-разному реагируют на лекарства.
Животные модели, в свою очередь, дороги, этически спорны и зачастую не могут предсказать реакцию человеческого организма, а это приводит к провалу многих многообещающих препаратов на поздних стадиях клинических испытаний.
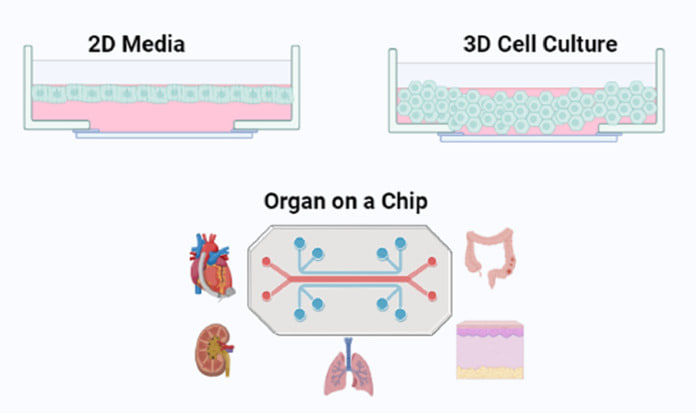
Технология «орган-на-чипе» как раз помогает решить эти проблемы. Это достижение клеточной биологии, материаловедения и микроинженерия, которые помогли создать миниатюрные, физиологически релевантные модели человеческих органов.
Таблица. Сравнительная характеристика 2D и 3D клеточных культур
| Характеристика | 2D-культура (монослой) | 3D-культура (объемная) |
| Морфология клеток | Клетки уплощены, вытянуты. Рост ограничен двумя измерениями, что приводит к неестественной поляризации и изменению цитоскелета. | Клетки сохраняют нативную (естественную) форму и полярность. Пролиферация и организация происходят в трех измерениях. |
| Взаимодействие со средой | Все клетки имеют равный и прямой доступ к питательным веществам, кислороду и лекарствам из среды. Клетки находятся в одной фазе роста. Газы диффундируют равномерно. | Клетки во внутренних слоях 3D-агрегата имеют ограниченный доступ к среде, что создает градиенты питания и кислорода. Из-за этого клетки находятся в разных фазах роста (пролиферирующие, зрелые, гипоксичные в центре). |
| Дифференцировка клеток | Дифференцировка клеток затруднена или происходит не полностью. Клетки часто дедифференцируются и теряют специфические функции. | 3D-микроокружение и межклеточные контакты способствуют правильной и более полной дифференцировке клеток. |
| Клеточные контакты | Формирование плотных и щелевых межклеточных контактов нарушено или отсутствует. Нет полноценного внеклеточного матрикса (ECM). | Наблюдается формирование реалистичных клеточных контактов (адгезивных, щелевых), а также взаимодействие клеток с внеклеточным матриксом (ECM). |
| Чувствительность к лекарствам | Клетки часто демонстрируют нереалистично высокую чувствительность к токсинам и лекарствам, что ведет к ложноположительным результатам при скрининге. | Клетки проявляют большую устойчивость к лекарствам, что более точно коррелирует с данными, полученными на животных моделях и в клинических исследованиях in vivo. |
| Визуализация и анализ | Процедуры окрашивания и микроскопии стандартизированы и просты. Высокое разрешение при съемке в плоскости X-Y. Анализ изображений не требует сложных алгоритмов. | Процедуры визуализации сложны и не стандартизированы. Требуется конфокальная микроскопия и сложный софт для 3D-реконструкции и анализа. Проникновение антител и красителей в глубокие слои затруднено. |
| Стоимость | Низкая. Не требует сложного оборудования и дорогих материалов. Легко масштабируется для высокопроизводительного скрининга. | Высокая. Требует специальных сред, матриц (гидрогелей, скаффолдов) и сложного оборудования для культивирования и анализа. |
Что такое «орган-на-чипе»?
«Орган-на-чипе» — это, кажется, просто клетки, посаженные на микрочип, но в данном случае мы говорим о сложной микроинженерной биомиметической системе, которая воспроизводит как структуру, так и функции человеческой ткани.
Берут прозрачный чип из полимера (чаще всего используется полидиметилсилоксан, PDMS), пронизанный микроканалами, по которым течет питательная жидкость, имитирующая кровоток. В этих каналах, на специальных пористых мембранах, выращиваются живые клетки — не в один слой, а в трехмерной структуре, часто из разных типов клеток, как в настоящем органе.

Ключевую роль в создании этих систем играют стволовые клетки, особенно индуцированные плюрипотентные стволовые клетки (iPSC). Именно они стали основным источником для получения кардиомиоцитов, нейронов, подоцитов и других специализированных клеток, позволяя создавать персонализированные модели заболеваний.
Пройдя путь от простых 2D-культур (с начала 1900-х годов) через 3D-культуры (конец 20-го века), исследователи пришли к пониманию, как важна динамика. Микрофлюидика — наука об управлении потоками жидкости в микромасштабе —позволяет создавать градиенты концентраций питательных веществ и кислорода, обеспечивает циркуляцию и удаление отходов, имитируя реальные физиологические процессы. И получается уже не просто «клетки-на-чипе», а именно «орган-на-чипе».
Лаборатория на чипе
Но просто воссоздать среду мало, еще нужно научиться взаимодействовать с мини-органами. Самой свежей новостью в этой области стала разработка исследователей из Швейцарской высшей технической школы Цюриха (ETH Zurich). Команда инженеров создала многофункциональную лабораторию-на-чипе, оснащенную микрозахватами. Они могут физически удерживать отдельные клетки или целые органоиды (миниатюрные версии органов, выращенные из стволовых клеток).
В чем же уникальность этой разработки:
- Интеграция с CMOS. Чип создан с использованием технологий, совместимых с комплементарной структурой металл-оксид-полупроводник (CMOS). Это означает, что на одном чипе можно легко интегрировать не только механические захваты, но и химические сенсоры, и электронику для стимуляции клеток.
- Сплав с памятью формы. Захваты изготовлены из многослойной структуры платины и титана — сплава с памятью формы. В ответ на электрический сигнал определенной полярности и величины «руки» захватов либо загибаются вверх, образуя клетку, либо распрямляются обратно на поверхность. Это происходит из-за изменения электрохимического состояния платины.
- Энергонезависимость. Огромное преимущество этих захватов в том, что после изменения формы они остаются в этом положении без дополнительной подачи энергии. Это контрастирует с оптическими или акустическими пинцетами, которые требуют постоянного энергопотребления и могут нагревать образцы.
- Мультимасштабность. На чипе расположен массив из девяти наборов микроклеток. В каждом наборе есть три захвата разного размера (с длиной «рук» 100, 150 и 280 микрометров), вложенных друг в друга. Самые маленькие предназначены для фиксации единичных клеток, а самые большие — для удержания целых органоидов.
- Встроенные сенсоры. Помимо захватов, чип содержит электрохимические сенсоры из золота, платины и палладия для обнаружения молекул, таких как нейромедиаторы. Использование разных материалов повышает чувствительность системы, и все они могут работать в электролитах, включая клеточные питательные среды.
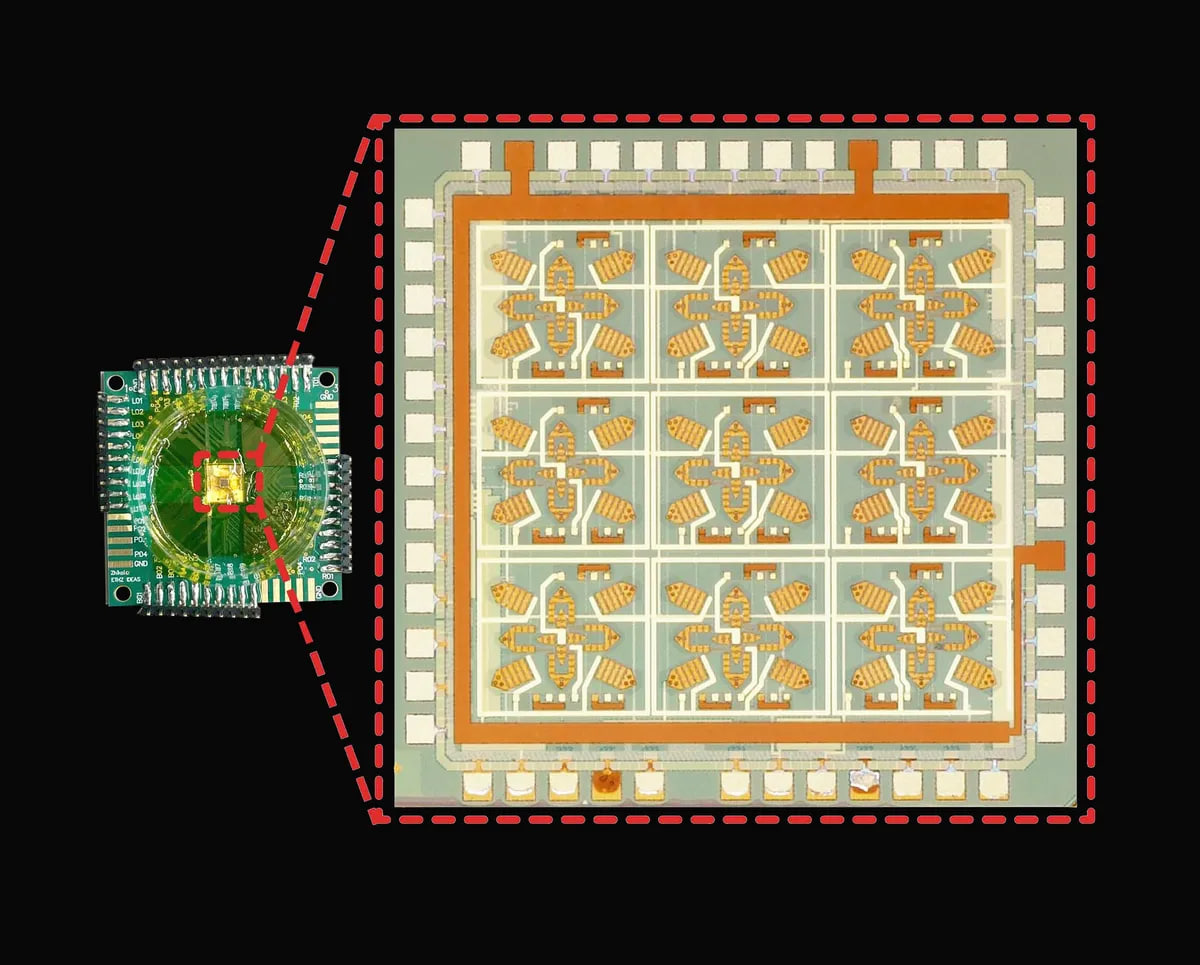
Первые тесты провели на стеклянных шариках, следующий шаг — демонстрация работы с живыми клетками. Такая система открывает путь к автоматизированному сближению тканей для их сращивания или длительному удержанию органоида под сенсором.
Какие органы на чипе уже выращивают?
Разработка лаборатории-на-чипе — это последнее из новшеств. За последние годы ученые создали десятки различных моделей «орган-на-чипе».
Легкие-на-чипе
Пионерская работа группы Дональда Ингбера из Института Висса Гарвардского университета в 2015 году. Их чип имитирует альвеолярно-капиллярную единицу легкого. Он состоит из двух каналов, разделенных пористой мембраной. В одном канале — воздух, в другом — «кровь», а на мембране растут клетки легких. Специальные вакуумные камеры по бокам позволяют растягивать мембрану, имитируя дыхательные движения.
На этой модели изучали отек легких, токсичность наночастиц и воздействие сигаретного дыма. Во время пандемии COVID-19 такие чипы использовались для тестирования противовирусных препаратов, включая гидроксихлорохин.
Мозг-на-чипе
Воссоздать полную структуру мозга невероятно сложно, но ученые успешно моделируют его отдельные функции. Существуют чипы для изучения гематоэнцефалического барьера (ГЭБ) — защитной стены между кровеносной системой и мозгом. Нарушения в работе ГЭБ связаны с неврологическими заболеваниями, такими как болезнь Хантингтона. Специализированные «спинной мозг-на-чипе» позволяют изучать взаимодействие нейронов и сосудов.
Сердце-на-чипе
Сердечно-сосудистые заболевания — главная причина смерти в мире, а из-за кардиотоксичности часто отзывают лекарств. Миниатюрные сердца из клеток в микрочипе, позволяют изучать электрофизиологию, реакцию на механическую стимуляцию и действие препаратов. Например, с их помощью можно увидеть, как увеличивается частота сокращений под действием изопротеренола, моделируя эффект адреналина.
Печень-на-чипе
Печень — главный «химический реактор» организма, и многие лекарства проваливаются именно из-за гепатотоксичности. Модели печени на чипе позволяют изучать метаболизм препаратов (например, парацетамола), их токсичность и даже такие заболевания, как неалкогольный стеатогепатит (NASH) и гепатит B. Важно, что такие системы поддерживают жизнеспособность клеток до 40 дней.
Почки-на-чипе
Модели почек помогают изучать вредное воздействие на почки таких препаратов, как цисплатин и гентамицин. Ученые также создают модели подоцитов — клеток, играющих ключевую роль в фильтрации крови, повреждение которых ведет к потере белка с мочой.
Кишечник-на-чипе
Этот чип имитирует ворсинки кишечника и позволяет изучать всасывание лекарств (фармакокинетику), взаимодействие с микробиотой и даже вирусные инфекции, например, вирус Коксаки.
Кожа-на-чипе
Многослойные модели кожи используются для тестирования косметики, изучения заживления ран, воспаления (например, вызванного TNF-α) и действия противовоспалительных препаратов (дексаметазон).
Концепция «человек-на-чипе» (Human-on-a-Chip) и рыночные перспективы
Следующий логический шаг — объединение нескольких «органов-на-чипе» в единую систему, которая будет имитировать взаимодействие органов в теле человека — «тело-на-чипе» (Body-on-a-chip) или «человек-на-чипе» (Human-on-a-chip). Уже существуют связки «кишечник-печень» для изучения всасывания и метаболизма, а также более сложные системы, включающие кишечник, печень и раковые клетки для тестирования противораковых препаратов.
Рынок органов на чипе
Потенциал технологии настолько велик, что привлек внимание регуляторов и гигантов фармацевтики. В 2017 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) заключило соглашение с компанией Emulate Inc. для оценки их технологии «органов-на-чипе». FDA также сотрудничает с Гарвардом в разработке средств против острой лучевой болезни.
Международная космическая станция (МКС) также задействована. В рамках проекта NCATS NASA на орбиту отправляют чипы с тканями легких, костного мозга, почек, чтобы изучить влияние микрогравитации на здоровье человека.
Рынок «органов-на-чипе» растет. В 2020 году его объем оценивался примерно в 41 миллион долларов США, а к концу 2026 года, по прогнозам, он достигнет 303,6 миллиона долларов. Ключевые игроки рынка — компании Emulate (США), Mimetas (Нидерланды), TissUse (Германия), TaraBiosystems (США) и многие другие.
Глобальная гонка в области разработки «органов-на-чипе» не обошла стороной и Россию. Активные исследования в этом направлении ведутся в Сибирском государственном медицинском университете (СибГМУ), где ученые работают над созданием отечественной тест-системы для персонализированной медицины.
Лекарства будущего будут создавать с учетом индивидуальных особенностей пациента, а значит, и испытывать их необходимо на адекватных биологических моделях, максимально точно воспроизводящих патологию конкретного человека.
Основной фокус разработки СибГМУ — создание микрофлюидной платформы для тестирования инновационных генотерапевтических препаратов. Ученые поставили перед собой задачу разработать модель вторичного опухолевого узла (метастаза) печени человека, совмещенную с микрофлюидным чипом. Технически проект предполагает создание органоида печени, в который будут внедрены единичные опухолевые клетки, имитирующие микрометастазы. Этот «мини-орган» затем интегрируется в микрофлюидный чип.
Что дальше
Технология «орган-на-чипе» уже достигла уровня зрелости, позволяющего применять ее в операционной среде, и готова к интеграции в доклинические испытания.
Конечно, предстоит решить еще много задач: стандартизировать протоколы, снизить стоимость, разработать высокопроизводительные системы для скрининга тысяч веществ одновременно, включить в модели микробиом и создать исчерпывающие системы «тело-на-чипе». Но путь уже примерно понятен, и мы движемся в правильном направлении.